La tinción de Ziehl Neelsen fue desarrollada inicialmente por Paul Ehrlich para poner de manifiesto la presencia de los bacilos causantes de la tuberculosis en muestras clínicas de pacientes.
Esta técnica es capaz de diferenciar los bacilos Acido Alcohol Resistentes (BAAR).
 La técnica de Z-N fuerza la penetración de la fucsina básica en la pared celular mediante la acción combinada del fenol y el calor, que aumentan la fluidez de la capa de ácidos micólicos: el calor “derrite” el componente ceroso y el fenol actúa a modo de disolvente, permitiendo el paso del colorante básico que se une a los ácidos micólicos con carga negativa. Cuando cesa la aplicación de calor y/o se elimina el exceso de fenol mediante un lavado con agua, la pared recupera su consistencia cerosa, pero las moléculas de fucsina quedan atrapadas en su espesor.
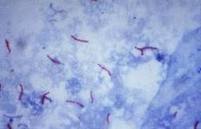
La técnica de Z-N fuerza la penetración de la fucsina básica en la pared celular mediante la acción combinada del fenol y el calor, que aumentan la fluidez de la capa de ácidos micólicos: el calor “derrite” el componente ceroso y el fenol actúa a modo de disolvente, permitiendo el paso del colorante básico que se une a los ácidos micólicos con carga negativa. Cuando cesa la aplicación de calor y/o se elimina el exceso de fenol mediante un lavado con agua, la pared recupera su consistencia cerosa, pero las moléculas de fucsina quedan atrapadas en su espesor.Con la coloración de Ziehl Neelsen se observan como bastoncitos delgados, ligeramente curvos, rojo fucsia, destacándose claramente contra el fondo azul.
· Coloración:
ü Disponer dos varillas de vidrio en forma paralela, a una distancia de aproximadamente 5 cm entre una y otra, una sobre un soporte dentro del lavabo/pileta de coloración.
ü Filtrar la cantidad de fucsina necesaria para las tinciones a realizar en la jornada. Si el número de baciloscopia a colorear es pequeño, se puede filtrar la fucsina directamente cuando se la deposita sobre el extendido a través de un pequeño embudo con papel de filtro.
ü Colocar sobre el soporte las láminas fijadas conservando el orden numérico con el extendido hacia arriba y manteniendo una separación de al menos 1cm entre ellas.
ü Cubrir totalmente la superficie del extendido con fucsina básica fenicada recién filtrada. Dispensar el colorante con suavidad, sin salpicar y sin tocar con el gotero o con el embudo los extendidos.
ü Con la llama de un hisopo embebido en alcohol calentar suavemente por debajo de los extendidos, con movimientos de vaivén, hasta que observe que se desprenden los primeros vapores blancos. No calentar con mechero.
ü En caso de derrame del colorante, reponer la fucsina, no dejar secar el preparado.
ü En el término de aproximadamente cinco minutos calentar tres veces hasta emisión de vapores; esto es suficiente para que la fucsina penetre adecuadamente en el bacilo y se fije a sus lípidos. No hervir la fucsina porque la pared de los bacilos puede destruirse y colorearse mal.
ü Con una pinza, levantar cuidadosamente la lámina portaobjetos desde el extremo más cercano al operador. Enjuagar con abundante agua a baja presión, con un frasco o un grifo. Lavar muy suave y cuidadosamente la superficie eliminando totalmente la solución de fucsina. Girar el extendido y lavar con cuidado también la parte posterior.
ü Inclinar el portaobjetos para eliminar el exceso de agua y así evitar diluir los reactivos que se utilizarán a continuación.
· Decoloración:
ü Cubrir la totalidad del extendido con solución decolorante y dejar actuar aproximadamente 3 minutos.
ü Enjuagar con abundante agua a baja presión.
ü Verificar que el extendido se ha decolorado (las partes más gruesas del extendido a lo sumo conservan un leve tinte rosado). Si se observan cúmulos rojos o coloración rosada intensa, volver a cubrir con solución decolorante, dejarla actuar entre uno y tres minutos y enjuagar nuevamente.
ü Eliminar el exceso de agua inclinando el portaobjetos
· Coloración de fondo:
ü Cubrir todo el extendido con solución de azul de metileno.
ü Dejar actuar durante un minuto.
ü Enjuagar las láminas en ambas caras con agua a baja presión y limpiar parte inferior con un algodón si ha quedado coloreada.
ü Observar si las láminas conservan la numeración clara y visible. Si no es así volver a numerarlas.
ü Dejar secar las láminas a temperatura ambiente, apoyándolas en posición vertical en un soporte sobre un papel absorbente. No apoyar papel absorbente sobre el extendido.
Qué buen artículo
ResponderEliminarEs lo más hermoso que he leído en la vida :,)
GRACIAS <3
excelente <3
ResponderEliminargracias